|

A cor que representa o metal na reciclagem é o amarelo.
Antes, muito antes que o homem aprendesse a gravar seus pensamentos pela escrita aprendeu a lidar com os metais.
Metais em estado puro são raros na natureza, sendo em geral encontrados em combinação com outros elementos e chamados, assim minérios.
Metais são elementos químicos que apresentam todas ou grande parte das seguintes propriedades físicas:
| ESTADO FÍSICO |
| Sólido |
na temperatura normal |
| Líquido |
Exceção "mercúrio" |
| CARACTERÍSTICAS DAS PRINCIPAIS LIGAS METÁLICAS |
| Denominação |
Composição |
Propriedades mecânicas |
| Bronze |
cobre 75-95% - estanho 25-5% |
Noxidável |
| Latão |
cobre 60 - 90% - zinco 40-10 % |
Resistência à água do mar e à tração |
| Duralumínio |
alumínio 96 % - cobre 3,5% - magnésio 0,5% |
Leveza e resistência |
| Hastelloy |
níquel 61% - molibdênio 28% - ferro 5,5% - cromo 1% |
Resistência à corrosão dos ácidos e bases |
| Chiorimet 3 |
níquel 63% - molibdênio 32% - ferro e cromo 3% |
Resistência aos agentes químicos oxidantes e redutores |
| Incomel |
níquel 80% - cromo 13% - ferro 7% |
Resistência à corrosão gasosa |
Os elementos metálicos mais comuns são os seguintes: alumínio, cádmio, cálcio, cromo, cobre, ouro, ferro, chumbo, manganês, mercúrio, níquel e zinco.
É possível combinar os elementos metálicos uns com os outros e também com outros elementos, formando compostos, soluções e misturas.
Uma mistura de dois ou mais metais ou de um metal e certos não metais, como o carbono, é chamada de liga.
Geralmente, os metais são duros e resistentes. Embora haja certas variações de um para o outro, os metais, usualmente, apresentam as seguintes propriedades:
- dureza ou resistência a serem riscados;
- resistência à ruptura;
- elasticidade;
- maleabilidade ou possibilidade de mudar de forma pela ação do martelo;
- resistência à fadiga e flexibilidade ou possibilidade de serem deformados sem sofrer rupturas.
fonte: Enciclopédia Conhecer
Podemos separá-los em dois tipos distintos, FERROSOS e NÃO FERROSOS:
FERROSOS
Principais tipos e aplicações na reciclagem:
- Ferro
- Vagões, ferramentas, utensílios, ferramentas, peças de carros, estruturas de edifícios, latas de bebidas e alimentos;
- Estamparia
- Estamparia solta, leve ou pesada, graúda ou miúda, sem revestimentos metálicos ou não metálicos, tais como zinco, chumbo, estanho, cobre, esmaltados, provenientes de Indústria Automobilística, Auto Peças, Eletro Doméstico ou similares. Inclui-se nesses tipos os rolos industriais obtidos pela industrialização de aparas de chapas ou bobinas e sobras de estampagem a quente e a frio.
- Cavaco
- Proveniente da Usinagem de Peças de Ferro, Aço e Ferro Fundido
- Granel pesada
- Materiais provenientes de desmonte de Instalações Industriais, veículos auto motores e máquinas industriais, Indústrias Petroquímicas, materiais ferroviários, Indústria Naval, demolições e de Indústria de Base, tais como: cantoneiras, tubos, vigas, chassis, eixos, transmissões, carcaças, tratores e implementos agrícolas, máquinas rodoviárias, trilhos usados em geral, telas pregos, engates, vagões, dormentes metálicos, rodeiros, puchantes, eixos ferroviários, navios e barcaças e sobras de trefilas.
- Ferro fundido
- Material composto de blocos de motores, peças fundidas, máquinas industriais, tubos, conexões, tampões, grelhas.
- Estamparia revestida
- Composta de folhas de flandres, litografados, embalagens e outras com revestimentos metálicos.
- Chaparia
- Material composto de: Paralamas, cabines de veículos, tampas e laterais de fogões, geladeIras, tambores, fitas de fardos, costaneiras, capas de fardo, arcos, galões e baldes.
- Mista
- Composta de vergalhões, cabos de aço, grade, para-choque, arames, coberturas.
Dos usos das sucatas ferrosas:
- No geral destinam-se a matéria-prima em siderurgia.
- Eventualmente alguns itens são retidos por sucateiros intermediários, para venda como material usado.
NÃO FERROSOS
Principais tipos e aplicações na reciclagem:
- Alumínio
- Latinhas de bebidas, janelas, portões, grades;
- Níquel
- Baterias de aparelhos celulares;
- Cobre encapado
- Fios com capa de isolação
- Cobre nú
- Chumbo
- redes de canalização, tanques e aparelhos de raios , lacres;
- Zinco
- placas das pilhas eletroquímicas secas;Telhas
fonte: MANUAL FERROVIÁRIO- FEPASA
Em Química um metal, do grego antigo métalon pode ser chamado de várias maneiras: pode ser um elemento, uma substância ou uma liga metálica caracterizado pela sua boa condutividade eléctrica e pelo seu calor, geralmente apresentando uma cor prateada ou amarelada, e uma elevada dureza. Qualquer metal pode ser definido também como um elemento químico que forma aglomerados de átomos com caráter metálico.
Num metal, cada átomo exerce apenas uma fraca atração nos eléctrons mais externos, da camada de valência, que podem então fluir livremente , proporcionando a formação de íons positivos e o estabelecimento de ligações iônicas com não-metais. Oseléctrons de valência são também responsáveis pela alta condutividade dos metais (teoria de bandas).
Os metais são um dos três grupos dos elementos distinguidos por suas propriedades de ionização e de ligação, junto com os metalóides (essa primeira classificação está caindo em desuso, por isso os metalóides foram revisados e alguns foram classificados como metais, e outros como ametais) e os não-metais. A maioria dos metais é quimicamente estável, com a exceção notável dos metais alcalinos e alcalino-terrosos, encontrados nas duas primeiras colunas à esquerda da tabela periódica. Alguns elementos antes classificados como metalóides, hoje são considerados metais, são esses o Germânio, Antimônio e Polônio, os demais são considerados ametais.
Características gerais
A condutividade térmica 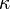 quantifica a habilidade dos materiais de conduzir calor. Materiais com alta condutividade térmica conduzem calor de forma mais rápida que os materiais com baixa condutividade térmica. A condutividade elétrica ( quantifica a habilidade dos materiais de conduzir calor. Materiais com alta condutividade térmica conduzem calor de forma mais rápida que os materiais com baixa condutividade térmica. A condutividade elétrica ( ) é usada para especificar o caráter elétrico de um material. Ela é o recíproco da resistividade. Ela é indicativa da facilidade com a qual um material é capaz de conduzir uma corrente elétrica. ) é usada para especificar o caráter elétrico de um material. Ela é o recíproco da resistividade. Ela é indicativa da facilidade com a qual um material é capaz de conduzir uma corrente elétrica.
Os metais são por natureza bons condutores térmicos e elétricos
A maleabilidade é uma propriedade que junto a ductilidade apresentam os corpos ao serem moldados por deformação. A diferença é que a ductilidade se refere a formação de filamentos e a maleabilidade permite a formação de delgadas lâminas do material sem que este se rompa, tendo em comum que não existe nenhum método para quantificá-los. Em muitos casos, a maleabilidade de uma substância metálica aumenta com a temperatura. Por isso, os metais são trabalhados mais facilmente a quente.
Os metais são fáceis de serem transformados em lâminas.
Elasticidade estuda o comportamento de corpos materiais que se deformam ao serem submetidos a ações externas (forças devidas ao contato com outros corpos, ação gravitacional agindo sobre sua massa, etc.), retornando à sua forma original quando a ação externa é removida. Até um certo limite ela depende do material e temperatura. A elasticidade linear, entretanto, é uma aproximação; os materiais reais exibem algum grau de comportamento não-linear.
Os metais apresentam alta capacidade de voltar ao normal após serem esticados.
O Brilho ou lustre é um termo que descreve o modo como a luz é refletida pela superfície de um mineral, ou qualquer outra superfície polida. A reflectividade de uma substância é dada pela razão entre a quantidade de luz reflectida e a quantidade de luz incidente. Os metais têm brilho, que recebe o nome característico de brilho metálico.
Cristalografia
Os metais apresentam grande diversidade de propriedades físicas e químicas, conforme a pressão, temperatura e outras variáveis, diferentes tipos de mecanismos e estruturas de cristalização, o que também lhe altera as características.
Geralmente, os metais apresentam ordenação cristalina simples, com alto nível de aglutinação atômica (o que implica alta densidade) e numerosos elementos de simetria. No que se refere às combinações, apresentam forte tendência a não formar compostos entre si, mas têm afinidade com elementos não metálicos como o oxigênio e o enxofre, com os quais formam, respectivamente, óxidos e sulfetos.
Metalografia
O tamanho, forma e disposição das partículas metálicas, especificados pela metalografia, são fundamentais para o reconhecimento das propriedades físicas que determinam aplasticidade, resistência à tração, dureza e outras propriedades do material. Esses fatores podem ser alterados por tratamentos térmicos (ciclos de aquecimento resfriamento controlados) ou mecânicos (forjamento, trefilação, laminação, etc.).
Com exceção do mercúrio, os metais se caracterizam por estarem no estado sólido em CNTP.
Tipos de metais
Os metais quando enumerados alcançam um total de cinquenta e sete elementos químicos, havendo grandes diferenças entre eles como mercúrio (que é líquido) e o sódio (que é leve). Os mais conhecidos e utilizados são o ferro, cobre, estanho, chumbo, ouro e a prata estes dois últimos classificados como metais preciosos.
É comum separar os metais em dois grandes grupos: os ferrosos (compostos por ferro) e os não-ferrosos (aonde o ferro está ausente).
Um outro grupo é composto pelos metais pesados que são metais quimicamente altamente reativos e bioacumuláveis. Como exemplos: cobalto, cobre, manganês, molibdênio, vanádio, estrôncio, e zinco.
A mistura de metais formam as ligas metálicas.
Relação dos metais existentes
Metais alcalinos
- Césio (Cs)
- Frâncio (Fr)
- Lítio (Li)
- Potássio (K)
- Rubídio (Rb)
- Sódio (Na)
Metais alcalino-terrosos
- Bário (Ba)
- Berílio (Be)
- Cálcio (Ca)
- Magnésio (Mg)
- Rádio (Ra)
- Estrôncio (Sr)
Metais de transição
- Prata (Ag, metal precioso)
- Bório (Bh)
- Cádmio (Cd)
- Cromo (Cr)
- Cobalto (Co)
- Copernicium (Cn)
- Cobre (Cu)
- Darmstácio (Ds)
- Dubnium (Db)
- Ferro (Fe)
- Háfnio (Hf)
- Hássio (Hs)
- Iridio (Ir)
- Manganês (Mn)
- Meitnério (Mt)
- Mercúrio (Hg)
- Molibdênio (Mo)
- Níquel (Ni)
- Nióbio (Nb)
- Ouro (Au, metal precioso)
- Ósmio (Os)
- Paládio (Pd, metal precioso)
- Platina (Pt, metal precioso)
- Rênio (Re)
- Ródio (Rh)
- Roentgenium (Rg)
- Ruténio (Ru)
- Rutherfordium (Rf)
- Escândio (Sc)
- Seabórgio (Sg)
- Tântalo (Ta)
- Tecnécio (Tc)
- Titânio (Ti)
- Tungstênio (W)
- Vanádio (V)
- Ítrio (Y)
- Zinco (Zn)
- Zircônio (Zr)
Outros metais
- Alumínio (Al)
- Bismuto (Bi)
- Estanho (Sn)
- Gálio (Ga)
- Índio (In)
- Chumbo (Pb)
- Tálio (Tl)
fonte: Wikipédia
|
